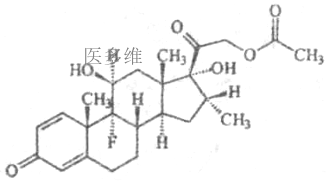
醋酸地塞米松片
本内容旨在为您提供一份关于西药类别中醋酸地塞米松片的详尽概览。醋酸地塞米松片的药理分类为肾上腺皮质激素类药,ATC分类为糖肾上腺皮质激素类,目前醋酸地塞米松片的国内上市企业有296家,包括钓鱼台医药集团吉林长青药业股份有限公司、山西敬德堂药业有限公司等。此外,还有更多关于醋酸地塞米松片的基本信息,如药品说明书、一致性评价情况、同成分全球研发现状...... 助您快速且全面地了解该药品。
- 药理分类: 激素及影响内分泌药/ 肾上腺皮质激素类药
- ATC分类: 系统用皮质甾体激素类/ 系统用皮质甾体激素类,单方/ 糖肾上腺皮质激素类
- 剂型: 片剂
- 医保类型: 甲类
- 是否2018年版基药品种: 是
- OTC分类: 处方药
- 是否289品种: 是
- 是否国家集采品种: 否
作用靶点
药品说明书
【说明书修订日期】
-
核准日期:2007年06月20日
修订日期:2016年05月17日
【成份】
【性状】
-
本品为白色片。
【适应症】
【规格】
-
0.75mg
【用法用量】
-
口服,成人开始剂量为一次0.75~3.00mg(1~4片),一日2~4次。维持量约一日0.75mg(1片),视病情而定。
【不良反应】
-
本品较大剂量易引起糖尿病、消化道溃疡和类柯兴综合征症状,对下丘脑-垂体-肾上腺轴抑制作用较强。并发感染为主要的不良反应。
【禁忌】
【注意事项】
【孕妇及哺乳期妇女用药】
-
妊娠期妇女使用可增加胎盘功能不全、新生儿体重减少或死胎的发生率,动物试验有致畸作用,应权衡利弊使用。乳母接受大剂量给药,则不应哺乳,防止药物经乳汁排泄,造成婴儿生长抑制、肾上腺功能抑制等不良反应。
【儿童用药】
-
小儿如使用肾上腺皮质激素,须十分慎重,用激素可抑制患儿的生长和发育,如确有必要长期使用时,应使用短效或中效制剂,避免使用长效地塞米松制剂。并观察颅内压的变化。
【老年用药】
-
易产生高血压,老年患者尤其是更年期后的女性使用易发生骨质疏松。
【药物相互作用】
【药物过量】
-
尚不明确。
【药理毒理】
-
肾上腺皮质激素类药,其抗炎、抗过敏、抗休克作用比泼尼松更显著,而对水钠潴留和促进排钾作用很轻,对垂体-肾上腺抑制作用较强。
1)抗炎作用:本产品可减轻和防止组织对炎症的反应,从而减轻炎症的表现。激素抑制炎症细胞,包括巨噬细胞和白细胞在炎症部位的集聚,并抑制吞噬作用、溶酶体酶的释放以及炎症化学中介物的合成和释放。可以减轻和防止组织对炎症的反应,从而减轻炎症的表现。
2)免疫抑制作用:包括防止或抑制细胞介导的免疫反应,延迟性的过敏反应,减少T淋巴细胞、单核细胞、嗜酸性细胞的数目,降低免疫球蛋白与细胞表面受体的结合能力,并抑制白介素的合成与释放,从而降低T淋巴细胞向淋巴母细胞转化,并减轻原发免疫反应的扩展。可降低免疫复合物通过基底膜,并能减少补体成分及免疫球蛋白的浓度。
【药代动力学】
-
本品极易自消化道吸收,其血浆T1/2为190分钟,组织T1/2为3日。血浆蛋白结合率较其他皮质激素类药物为低。
【贮藏】
-
遮光,密封保存。
【包装】
-
口服固体药用高密度聚乙烯瓶,每瓶100片。
【有效期】
-
24个月
【执行标准】
-
《中国药典》2015年版二部
【批准文号】
-
国药准字H41022090
【生产企业】
说明书修订日期
药品名称
成份
性状
适应症
规格
用法用量
不良反应
禁忌
注意事项
孕妇及哺乳期妇女用药
儿童用药
老年用药
药物相互作用
药物过量
药理毒理
药代动力学
贮藏
包装
有效期
执行标准
批准文号
生产企业

查看更多药品说明书,请前往“合理用药”平台
国内上市情况
| 批准文号 | 药品名称 | 规格 | 剂型 | 生产单位 | 上市许可持有人 | 药品类型 | 国产或进口 | 批准日期 |
|---|---|---|---|---|---|---|---|---|
|
国药准字H22022266
|
醋酸地塞米松片
|
0.75mg
|
片剂
|
吉林省贝克药业有限公司
|
—
|
化学药品
|
国产
|
2002-09-13
|
|
国药准字H23021001
|
醋酸地塞米松片
|
0.75mg
|
片剂
|
黑龙江百泰药业有限公司
|
—
|
化学药品
|
国产
|
2002-09-13
|
|
国药准字H34020320
|
醋酸地塞米松片
|
0.75mg
|
片剂
|
芜湖三益制药有限公司
|
—
|
化学药品
|
国产
|
2002-07-10
|
|
国药准字H34020800
|
醋酸地塞米松片
|
0.75mg
|
片剂
|
合肥三河制药有限公司
|
—
|
化学药品
|
国产
|
2002-08-16
|
|
国药准字H34021513
|
醋酸地塞米松片
|
0.75mg
|
片剂
|
安徽省淮北药业有限责任公司
|
—
|
化学药品
|
国产
|
2002-08-16
|

查看更多国内药品批文及详细数据,请前往“摩熵医药企业版”平台
同成分全球上市情况
| 药品名称 | 公司名称 | 申请号/批准号 | 规格 | 剂型/给药途径 | 上市国家/地区 | 市场状态 | 日期 |
|---|---|---|---|---|---|---|---|
|
醋酸地塞米松片
|
吉林省贝克药业有限公司
|
国药准字H22022266
|
750μg
|
片剂
|
中国
|
已过期
|
2002-09-13
|
|
醋酸地塞米松片
|
黑龙江百泰药业有限公司
|
国药准字H23021001
|
750μg
|
片剂
|
中国
|
已过期
|
2002-09-13
|
|
醋酸地塞米松片
|
芜湖三益制药有限公司
|
国药准字H34020320
|
750μg
|
片剂
|
中国
|
已过期
|
2002-07-10
|
|
醋酸地塞米松片
|
合肥三河制药有限公司
|
国药准字H34020800
|
750μg
|
片剂
|
中国
|
已过期
|
2002-08-16
|
|
醋酸地塞米松片
|
安徽省淮北药业有限责任公司
|
国药准字H34021513
|
750μg
|
片剂
|
中国
|
已过期
|
2002-08-16
|

查看药品全球上市情况及详细数据,请前往“摩熵医药企业版”平台
药品中标情况
- 最低中标价0.01
- 规格:750μg
- 时间:2012-07-10
- 省份:广东
- 企业名称:遂成药业股份有限公司
- 最高中标价0
- 规格:700μg
- 时间:2019-12-16
- 省份:山东
- 企业名称:AbbVie Deutschland GmbH & Co.KG
| 药品名称 | 剂型 | 规格 | 转化系数 | 最小制剂单位价格(元) | 价格(元) | 生产企业 | 投标企业 | 省份 | 公布时间 | 网页链接 |
|---|---|---|---|---|---|---|---|---|---|---|
|
醋酸地塞米松片
|
片剂
|
750μg
|
100
|
0.35
|
35
|
福州海王福药制药有限公司
|
福州海王福药制药有限公司
|
云南
|
2020-04-30
|
无 |
|
醋酸地塞米松片
|
片剂
|
750μg
|
100
|
0.16
|
16
|
西南药业股份有限公司
|
西南药业股份有限公司
|
云南
|
2020-04-30
|
无 |
|
地塞米松磷酸钠注射液
|
注射剂
|
1ml:5mg
|
1
|
0.2
|
0.1976
|
国药集团容生制药有限公司
|
国药集团容生制药有限公司
|
宁夏
|
2017-03-16
|
无 |
|
地塞米松磷酸钠注射液
|
注射剂
|
1ml:2mg
|
1
|
0.15
|
0.15
|
开封制药(集团)有限公司
|
开封制药(集团)有限公司
|
宁夏
|
2017-03-16
|
无 |
|
地塞米松磷酸钠注射液
|
注射剂
|
1ml:5mg
|
1
|
0.21
|
0.2098
|
开封制药(集团)有限公司
|
开封制药(集团)有限公司
|
宁夏
|
2017-03-16
|
无 |

查看更多药品招投标情况及详细数据,请前往“摩熵医药企业版”平台
国家集中采购情况
| 药品名称 | 中选企业 | 剂型 | 规格包装 | 采购周期 | 中选价格(元) | 国家集采批次 | 公布日期 |
|---|---|---|---|---|---|---|---|
|
醋酸地塞米松片
|
安徽金太阳生化药业有限公司
|
片剂
|
100片/瓶
|
1.5年
|
10.5
|
—
|
2025-10-29
|
|
醋酸地塞米松片
|
新乡市常乐制药有限责任公司
|
素片
|
100片/瓶
|
1.5年
|
4.9
|
—
|
2025-10-29
|
|
醋酸地塞米松片
|
浙江仙琚制药股份有限公司
|
素片
|
100片/瓶
|
1.5年
|
10.8
|
—
|
2025-10-29
|
|
醋酸地塞米松片
|
广东恒健制药有限公司
|
片剂
|
100片/瓶
|
1.5年
|
4.6
|
—
|
2025-10-29
|
|
醋酸地塞米松片
|
湖南中南制药有限责任公司
|
素片
|
100片/瓶
|
1.5年
|
4.48
|
—
|
2025-10-29
|

查看更多药品国家集中采购情况及详细数据,请前往“摩熵医药企业版”平台
一致性评价
| 企业 | 品种 | 规格 | 剂型 | 过评情况 | 过评时间 | 注册分类 |
|---|---|---|---|---|---|---|
|
安徽金太阳生化药业有限公司
|
醋酸地塞米松片
|
750μg
|
片剂
|
通过
|
2023-04-11
|
无注册分类
|
|
辰欣药业股份有限公司
|
醋酸地塞米松片
|
750μg
|
片剂
|
通过
|
2024-07-12
|
无注册分类
|
|
浙江仙琚制药股份有限公司
|
醋酸地塞米松片
|
|
片剂
|
通过
|
2025-10-13
|
无注册分类
|
|
津药药业股份有限公司
|
醋酸地塞米松片
|
750μg
|
片剂
|
通过
|
2022-07-04
|
无注册分类
|
|
新乡市常乐制药有限责任公司
|
醋酸地塞米松片
|
750μg
|
片剂
|
通过
|
2024-11-12
|
无注册分类
|

查看更多过评企业情况及详细数据,请前往“摩熵医药企业版”平台
同成分全球研发现状
| 药物名称 | 研发代码 | 首家研发企业 | 参与研发企业 | 治疗领域 | 适应症(中) | 全球最高研发阶段 | 中国最高研发阶段 | 靶点(简化靶点) |
|---|---|---|---|---|---|---|---|---|
|
—
|
NDF-SI01
|
韩国中央大学
|
韩国中央大学
|
眼科
|
眼部疾病
|
查看 | 查看 |
|
|
地塞米松
|
101-PGC-005;CD-102;EGP-437;ENV-1105;FT-4145;IBE-814;IBI-10090;ISV-305;IVMED-10;IVMED-20;OC-118;OCS-01;OTO-104;OTX-DED;TLC-x99
|
—
|
|
免疫调节;感染
|
COVID-19;幼年特发性关节炎
|
查看 | 查看 |
GCCR
|
|
地塞米松
|
OTO-104
|
—
|
|
杂类
|
|
查看 | 查看 |
GCCR
|
|
地塞米松
|
|
—
|
|
中毒/药物成瘾;免疫调节;感染;炎症
|
COVID-19;义膜性喉炎;化疗后呕吐;超敏反应
|
查看 | 查看 |
GCCR;PLA2
|
|
地塞米松
|
ISV-305
|
—
|
|
眼科;神经系统
|
|
查看 | 查看 |
|

查看更多全球研发现状情况及详细数据,请前往“摩熵医药企业版”平台
国内药品注册申报情况
| 受理号 | 药品名称 | CDE企业名称 | 申请类型 | 注册类型 | 承办日期 | 状态开始日期 | 办理状态 | 审评结论 |
|---|---|---|---|---|---|---|---|---|
|
CYHB2400613
|
醋酸地塞米松片
|
吉林恒星科技制药有限公司
|
补充申请
|
—
|
2024-05-11
|
—
|
—
|
查看 |
|
CYHB2500151
|
醋酸地塞米松片
|
安徽金太阳生化药业有限公司
|
补充申请
|
—
|
2025-01-17
|
—
|
—
|
— |
|
CYHB2550229
|
醋酸地塞米松片
|
河南润弘制药股份有限公司
|
补充申请
|
—
|
2025-06-14
|
—
|
—
|
— |
|
CYHB2050715
|
醋酸地塞米松片
|
天津天药药业股份有限公司
|
补充申请
|
—
|
2020-11-18
|
2022-07-07
|
制证完毕-已发批件
|
查看 |
|
CYHB2201538
|
醋酸地塞米松片
|
河南润弘本草制药有限公司
|
补充申请
|
—
|
2022-08-24
|
—
|
—
|
查看 |

查看更多药品审评情况及详细数据,请前往“摩熵医药企业版”平台
国内药品临床试验登记
| 登记号 | 试验专业题目 | 药物名称 | 适应症 | 试验状态 | 试验分期 | 申办单位 | 试验机构 | 首次公示日期 |
|---|---|---|---|---|---|---|---|---|
|
CTR20211266
|
醋酸地塞米松片在空腹及餐后给药条件下随机、开放、单剂量、两周期双交叉生物等效性试验
|
醋酸地塞米松片
|
主要用于过敏性与自身免疫性炎症性疾病。如结缔组织病,严重的支气管哮喘,皮炎等过敏性疾病,溃疡性结肠炎,急性白血病,恶性淋巴瘤等。此外,本药还用于某些肾上腺皮质疾病的诊断——地塞米松抑制试验。
|
已完成
|
BE试验
|
安徽金太阳生化药业有限公司
|
蚌埠医学院第一附属医院
|
2021-06-09
|
|
CTR20200468
|
DM001随机、开放、单剂量、两制剂、两周期、交叉设计在健康人体空腹和餐后状态下生物等效性试验
|
醋酸地塞米松片
|
适用于过敏性与自身免疫性炎症性疾病,如结缔组织病,严重的支气管哮喘,皮炎等过敏性疾病,溃疡性结肠炎,急性白血病,恶性淋巴瘤等。
|
已完成
|
BE试验
|
天津天药药业股份有限公司
|
洛阳市中心医院
|
2020-04-07
|
|
CTR20244859
|
醋酸地塞米松片在空腹及餐后条件下的人体生物等效性试验
|
醋酸地塞米松片
|
可用于治疗多种炎症或过敏性疾病。高剂量时,本品可抑制免疫反应,因此也可用于预防或治疗器官移植排斥。
|
已完成
|
BE试验
|
湖南中南制药有限责任公司
|
湖南医药学院第一附属医院
|
2024-12-23
|
|
CTR20232986
|
醋酸地塞米松片在健康受试者中单中心、随机、开放、两制剂、单次给药、两周期、双交叉空腹/餐后生物等效性试验
|
醋酸地塞米松片
|
主要用于过敏性与自身免疫性炎症性疾病。如结缔组织病,严重的支气管哮喘,皮炎等过敏性疾病,溃疡性结肠炎,急性白血病,恶性淋巴瘤等。此外,本药还用于某些肾上腺皮质疾病的诊断——地塞米松抑制试验。
|
已完成
|
BE试验
|
新乡市常乐制药有限责任公司
|
武汉市肺科医院
|
2023-09-22
|
|
CTR20210026
|
醋酸地塞米松片在健康受试者中的随机、开放、两制剂、单次给药、两周期、交 叉、空腹和高脂餐后人体生物等效性研究
|
醋酸地塞米松片
|
主要用于过敏性与自身免疫性炎症性疾病。如结缔组织病,严重的支气管哮喘,皮炎等过敏性疾病,溃疡性结肠炎,急性白血病,恶性淋巴瘤等。此外,本品还用于某些肾上腺皮质疾病的诊断如地塞米松抑制试验。
|
进行中
|
BE试验
|
浙江仙琚制药股份有限公司
|
重庆三峡医药高等专科学校附属医院
|
2021-04-06
|

查看更多中国临床试验情况及详细数据,请前往“摩熵医药企业版”平台