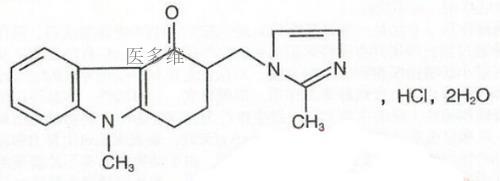
盐酸昂丹司琼氯化钠注射液
本内容旨在为您提供一份关于西药类别中盐酸昂丹司琼氯化钠注射液的详尽概览。盐酸昂丹司琼氯化钠注射液的药理分类为抗肿瘤辅助药,ATC分类为5-羟色胺拮抗药,目前盐酸昂丹司琼氯化钠注射液的国内上市企业有14家,包括广东南国药业有限公司、山东齐都药业有限公司等。此外,还有更多关于盐酸昂丹司琼氯化钠注射液的基本信息,如一致性评价情况、国内药品注册申报情况、国内药品临床试验登记...... 助您快速且全面地了解该药品。
- 药理分类: 抗肿瘤药/ 抗肿瘤辅助药
- ATC分类: 镇吐药和止呕药/ 镇吐药和止呕药/ 5-羟色胺拮抗药
- 剂型: —
- 医保类型: —
- 是否2018年版基药品种: ——
- OTC分类: ——
- 是否289品种: ——
- 是否国家集采品种: ——
药品说明书
【说明书修订日期】
-
核准日期:2007年4月23日
【警告】
-
警示语
1、本品使用前请详细检查,如有溶液浑浊、异物、封口松动、漏液、瓶身或瓶口裂纹者,请勿使用。
2、本品一经使用,必须一次性用完。
【药品名称】
-
通用名称: 盐酸昂丹司琼氯化钠注射液
英文名称:Ondansetron Hydrochloride and Sodium Chloride Injection
汉语拼音:Yansuan Angdansiqiong Luhuana Zhusheye
【成份】
【性状】
-
本品为无色或几乎无色的澄明液体。
【适应症】
【规格】
【用法用量】
-
本品供静脉滴注用药。给药剂量和途径视呕吐严重程度而定。成人剂量一般每天8mg。对于高度催吐的化疗药引起的呕吐,在化疗前30分钟,化疗后4小时,8小时各静脉滴注本品8mg,停止化疗以后每8-12小时口服片剂8mg;对于催吐程度不太强的化疗药引起的呕吐,化疗前30分钟静脉滴注本品8mg,以后每8-12小时口服片剂8mg,连续5天;对放射治疗引起的呕吐,首剂应于放疗前1-2小时口服片剂8mg,以后每8小时口服8mg。用于预防和治疗手术后呕吐,成人可于麻醉诱导同时静脉滴注本品4mg,对于已出现术后呕吐,可缓慢静脉滴注本品4mg进行治疗。输液时间应不小于15分钟。
【不良反应】
【禁忌】
-
对本品有过敏反应者禁用。胃肠道梗阻者禁用。
【注意事项】
【孕妇及哺乳期妇女用药】
-
本品在人类怀孕期间使用的安全性尚未确定,对动物试验研究未显示对胚胎期、胎儿形成期、妊娠期、围产期及产后期有直接或间接害处。然而由于对动物的研究并不完全能够预示人的反应,故不推荐人在怀孕期特别是头3个月内间使用本品。实验显示,本品可由授乳动物乳汁中分泌,故采用本品时暂停母乳喂养。
【儿童用药】
-
据国外临床研究文献报道,四岁以上儿童可耐受本品,于化疗前静脉滴注5mg/m2(按体表面积)的剂量,化疗后12小时后再继续口服给药,每次4mg,每日两次,连服5天。
为了预防接受全身麻醉手术的儿童患者出现术后恶心和呕吐,应在诱导麻醉前、期间或之后用本品以0.1mg/kg的剂量或最大剂量4mg,缓慢静脉滴注。对于儿童患者已出现的术后恶心、呕吐,可用本品0.1mg/kg或最大4mg的剂量缓慢静脉滴注。
【老年用药】
-
老年人由于代谢减慢,消除半衰期延长(5小时),口服生物利用度提高(65%)但无临床意义。65岁以上的用药疗程及对药物的耐受性与青年人的一样,无须调整剂量及用药途径。
【药物相互作用】
【药物过量】
【药理毒理】
-
药理作用:本品是一种选择性的5-羟色胺3(5-HT3)受体拮抗剂。其作用机理尚不完全明确,可能是通过拮抗外周迷走神经末梢和中枢化学感受区中的5-HT3受体,从而阻断因化疗和手术等因素促进小肠嗜铬细胞释放5-羟色胺,兴奋迷走传入神经而导致的呕吐反射。本品选择性较高,无锥体外系反应、过度镇静等副作用。
毒理研究:
生殖毒性:本品经口给药剂量达15mg/kg/天时,对雄性和雌性大鼠的生育力和一般生殖行为无明显影响。动物试验结果未表现出致畸胎作用。妊娠大鼠和家兔本品静脉给药剂量达4mg/kg/天时,未表现出对生育力和胎仔的损害作用。但尚无充分和严格对照的妊娠妇女给药的临床研究。由于动物试验并不总能预测药品对人体的影响,故只有在确实需要时,才可以在妊娠期间服用本品。
本品可通过大鼠乳汁分泌,但尚不清楚其是否通过人乳汁分泌。因为许多药物可经乳汁排泄,故哺乳妇女服用本品时应慎重考虑其对后代的影响。
遗传毒性:本品在标准遗传毒性试验中均未表现出致突变性。
致癌性:在给药2年的试验中,大鼠和小鼠经口给予本品的剂量分别达10mg/kg/天和30mg/kg/天,结果未表现出致癌作用。
【药代动力学】
【贮藏】
-
遮光,密闭保存。
【包装】
-
(1)玻璃输液瓶,100ml/瓶;50ml/瓶;(2)非PVC多层共挤输液用袋单阀,100ml/袋;50ml/袋;(3)非PVC多层共挤输液用袋双阀,100ml/袋;50ml/袋;(4)非PVC多层共挤输液用袋双阀双层无菌,100ml/袋;50ml/袋;(5)三层共挤输液用袋,100ml/袋;(6)聚丙烯输液瓶,100ml/瓶。
【有效期】
-
(1)玻璃输液瓶包装:暂定12个月;(2)非PVC多层共挤输液用袋包装:暂定12个月;(3)三层共挤输液用袋:18个月;(4)聚丙烯输液瓶,24个月。
【执行标准】
-
YBH01592003
【批准文号】
-
(1)100ml:国药准字H20030509
(2)50ml:国药准字H20060398
【生产企业】
-
企业名称:山东齐都药业有限公司
生产地址:淄博市临淄区宏达路17号
邮政编码:255400
电话号码:0533-7150888 7181600
传真号码:0533-7186426 7181635
网 址:http://www.qidu-pharma.com
说明书修订日期
警告
药品名称
成份
性状
适应症
规格
用法用量
不良反应
禁忌
注意事项
孕妇及哺乳期妇女用药
儿童用药
老年用药
药物相互作用
药物过量
药理毒理
药代动力学
贮藏
包装
有效期
执行标准
批准文号
生产企业

查看更多药品说明书,请前往“合理用药”平台
国内上市情况
| 批准文号 | 药品名称 | 规格 | 剂型 | 生产单位 | 上市许可持有人 | 药品类型 | 国产或进口 | 批准日期 |
|---|---|---|---|---|---|---|---|---|
|
国药准字H20040650
|
盐酸昂丹司琼氯化钠注射液
|
100ml:昂丹司琼8mg与氯化钠0.9g
|
注射剂
|
江苏豪森药业集团有限公司
|
江苏豪森药业集团有限公司
|
化学药品
|
国产
|
2025-05-26
|
|
国药准字H20060398
|
盐酸昂丹司琼氯化钠注射液
|
50ml:昂丹司琼8mg与氯化钠0.45g
|
注射剂
|
山东齐都药业有限公司
|
山东齐都药业有限公司
|
化学药品
|
国产
|
2025-02-25
|
|
国药准字H20041406
|
盐酸昂丹司琼氯化钠注射液
|
100ml:昂丹司琼8mg与氯化钠0.9g
|
注射剂
|
广东南国药业有限公司
|
广东南国药业有限公司
|
化学药品
|
国产
|
2024-12-24
|
|
国药准字H20040164
|
盐酸昂丹司琼氯化钠注射液
|
100ml:昂丹司琼8mg与氯化钠0.9g
|
注射剂
|
威海爱威制药有限公司
|
—
|
化学药品
|
国产
|
2015-06-23
|
|
国药准字H20040529
|
盐酸昂丹司琼氯化钠注射液
|
100ml:昂丹司琼8mg与氯化钠0.9g
|
注射剂
|
湖南康都制药有限公司
|
—
|
化学药品
|
国产
|
2004-04-12
|

查看更多国内药品批文及详细数据,请前往“摩熵医药企业版”平台
同成分全球上市情况
| 药品名称 | 公司名称 | 申请号/批准号 | 规格 | 剂型/给药途径 | 上市国家/地区 | 市场状态 | 日期 |
|---|---|---|---|---|---|---|---|
|
盐酸昂丹司琼氯化钠注射液
|
广东南国药业有限公司
|
国药准字H20041406
|
100ml:8mg/900mg
|
注射剂
|
中国
|
在使用
|
2024-12-24
|
|
盐酸昂丹司琼氯化钠注射液
|
山东齐都药业有限公司
|
国药准字H20060398
|
50ml:8mg/450mg
|
注射剂
|
中国
|
在使用
|
2025-02-25
|
|
盐酸昂丹司琼氯化钠注射液
|
江苏豪森药业集团有限公司
|
国药准字H20040650
|
100ml:8mg/900mg
|
注射剂
|
中国
|
在使用
|
2025-05-26
|
|
盐酸昂丹司琼氯化钠注射液
|
威海爱威制药有限公司
|
国药准字H20040164
|
100ml:8mg/900mg
|
注射剂
|
中国
|
已过期
|
2015-06-23
|
|
盐酸昂丹司琼氯化钠注射液
|
湖南康都制药有限公司
|
国药准字H20040529
|
100ml:8mg/900mg
|
注射剂
|
中国
|
已过期
|
2004-04-12
|

查看药品全球上市情况及详细数据,请前往“摩熵医药企业版”平台
药品中标情况
- 最低中标价0.84
- 规格:2ml:4mg
- 时间:2023-05-12
- 省份:云南
- 企业名称:瑞阳制药股份有限公司
- 最高中标价0
- 规格:4ml:8mg
- 时间:2011-04-26
- 省份:上海
- 企业名称:Novartis Pharma Schweiz AG
| 药品名称 | 剂型 | 规格 | 转化系数 | 最小制剂单位价格(元) | 价格(元) | 生产企业 | 投标企业 | 省份 | 公布时间 | 网页链接 |
|---|---|---|---|---|---|---|---|---|---|---|
|
盐酸昂丹司琼片
|
片剂
|
4mg
|
10
|
10.7
|
107
|
福安药业集团宁波天衡制药有限公司
|
福安药业集团宁波天衡制药有限公司
|
山西
|
2015-08-31
|
无 |
|
盐酸昂丹司琼氯化钠注射液
|
注射剂
|
8mg
|
1
|
30.18
|
30.178
|
山东齐都药业有限公司
|
—
|
广东
|
2015-04-03
|
无 |
|
盐酸昂丹司琼氯化钠注射液
|
注射剂
|
100ml:8mg/900mg
|
1
|
27.33
|
27.33
|
山东齐都药业有限公司
|
山东齐都药业有限公司
|
江苏
|
2020-04-30
|
无 |
|
盐酸昂丹司琼氯化钠注射液
|
注射剂
|
100ml:8mg/900mg
|
1
|
19.59
|
19.59
|
威海爱威制药有限公司
|
—
|
湖北
|
2017-04-17
|
无 |
|
盐酸昂丹司琼注射液
|
注射剂
|
2ml:4mg
|
1
|
8.92
|
8.918
|
华润双鹤利民药业(济南)有限公司
|
华润双鹤利民药业(济南)有限公司
|
宁夏
|
2017-03-16
|
无 |

查看更多药品招投标情况及详细数据,请前往“摩熵医药企业版”平台
国家集中采购情况
同成分全球研发现状
国内药品注册申报情况
| 受理号 | 药品名称 | CDE企业名称 | 申请类型 | 注册类型 | 承办日期 | 状态开始日期 | 办理状态 | 审评结论 |
|---|---|---|---|---|---|---|---|---|
|
CYHB1409650
|
盐酸昂丹司琼氯化钠注射液
|
百正药业股份有限公司
|
补充申请
|
—
|
2015-02-28
|
2016-04-07
|
制证完毕-已发批件河南省 1008482783619
|
查看 |
|
CXHB0502462
|
盐酸昂丹司琼氯化钠注射液
|
上海华源长富药业(集团)有限公司
|
补充申请
|
—
|
2005-12-08
|
2015-08-21
|
制证完毕-已发批件
|
— |
|
CXS20020648
|
盐酸恩丹西酮氯化钠注射液
|
大同市惠达药业有限责任公司
|
新药
|
4
|
2003-11-20
|
2004-04-16
|
已发批件 山西省
|
— |
|
CYHB1410311
|
盐酸昂丹司琼氯化钠注射液
|
石家庄四药有限公司
|
补充申请
|
—
|
2015-03-14
|
2016-05-31
|
制证完毕-已发批件河北省 1013577252420
|
查看 |
|
X0402105
|
盐酸昂丹司琼氯化钠注射液
|
石家庄四药股份有限公司
|
补充申请
|
—
|
2004-04-21
|
2004-08-20
|
已发批件河北省
|
查看 |

查看更多药品审评情况及详细数据,请前往“摩熵医药企业版”平台